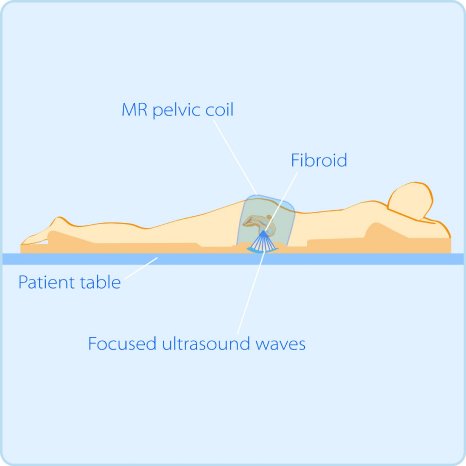
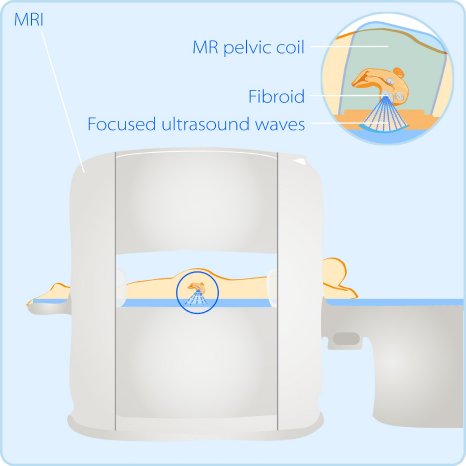
Die so genannte HIFU-Einheit ist in die Tischplatte eines Magnetresonanz-Tomographen integriert. Durch eine spezielle Anordnung der Ultraschall-Quellen durchdringt der Schall die Haut des Patienten ohne sie zu beschädigen und entwickelt erst in der Tiefe durch seine Bündelung die Wirkung. Dort erwärmt sich das Gewebe im Zielgebiet bis auf 70 Grad und stirbt ab. Die ständige Echtzeit-Bildkontrolle mittels Magnetresonanztomographie bietet dem Behandler dabei eine wichtige Kontrolle über den Therapieverlauf und ihren Erfolg. Für den Patienten ist die ca. zwei Stunden dauernde Prozedur vollkommen schmerzfrei.
Bisher wurde von Philips Healthcare ein MR-HIFU Gerät zur Behandlung von Uterusmyomen (gutartige Geschwülste in der Gebärmutter-Muskulatur) entwickelt. Dieses befindet sich derzeitig in der klinischen Erprobung. "Die ersten Ergebnisse sind vielversprechend", berichtet Thomas Andreae, Direktor MR Marketing Emerging Systems & Therapy für Philips Healthcare. "Die HIFU-Therapie ist für die Patientinnen viel weniger belastend und deutlich risikoärmer als die heute bei Uterusmyomen übliche Kleinst-Operation oder eine Entfernung der Gebärmutter als Ganzes"
Jetzt gilt es für die Forscher und Entwickler das Anwendungsspektrum auf andere Krankheitsbilder zu erweitern. Es zeichnet sich bereits ab, dass zukünftig auch komplexere Eingriffe denkbar sind, z. B. das Behandeln bösartiger Tumore wie Mamma- oder Prostata-Karzinome. Die Philips-Forschung hat in Zusammenarbeit mit der Gruppe von Prof. Chrit Moonen, Universität Bordeaux, für dieses wichtige klinische Einsatzgebiet bereits weiterführende und vielversprechende Technologien entwickelt. Zum einen kann mit diesen Lösungen eine absolut homogene Temperaturverteilung erreicht werden, die für das vollständige Abtöten von Tumorgewebe zwingend nötig ist, und zum Anderen muss die HIFU-Einheit die Fähigkeit besitzen auch große Areale zu erreichen.
Ein weiteres Einsatzgebiet kann zukünftig auch die örtliche Gabe von Medikamenten am Krankheitsherd (local drug delivery) sein. Mit Medikamenten beladene Lipid-Kügelchen werden in den Blutkreislauf injiziert. Das Tumorgebiet wird mittels High Focused Ultraschall leicht aufgeheizt. Die lokale Wärme im Gewebe macht die Oberfläche der Lipid-Kügelchen porös und die Medikamente werden ausgeschüttet. Hoch konzentriert gelangen dabei die Wirkstoffe in Tumornähe und könnten ihre Wirkung vor Ort wesentlich besser entfalten als z.B. bei einer systemischen Medikamenten-Therapie.
Weltweit befinden sich bereits zehn Systeme für die klinische Erprobung im Einsatz.