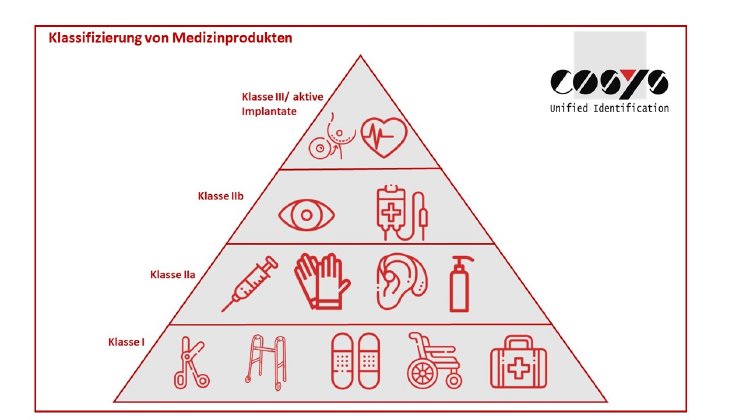
Klassifizierung ist ein weiterer wichtiger Punkt der Verordnung. Die Medizinprodukte müssen in unterschiedliche Klassen eingeteilt werden. Die Einteilung erfolgt nach dem Risikopotential der Produkte für den menschlichen Körper. Die Produkte werden in 4 Gruppen eingeteilt von niedriges bis hohes Risikopotential.
Klasse III
Die Klasse III stellt die Klasse mit dem höchsten Risikopotenzial dar. In dieser Klasse sind Großteiles die Produkte, welche in den menschlichen Körper eingesetzt werden. In diese Klasse fallen unter anderem Herzschrittmacher, Herzklappen, Herz- und Ablationskatheter, Hüft-, Schulter- und Kniegelenksprothesen, Brustimplantate, intrakranielle Stents und koronare Stents.
Die Übergangsfrist endet am 25. Mai 2020.
Klasse IIb
Alle Produkte mit erhöhtem Risikopotenzial befinden sich in der Klasse IIb. In dieser Klasse befinden sich Produkte und Geräte, die hohe Sicherheitsstandards benötigen, weil sie wichtig für den Patienten sind. Unteranderem periphere Gefäßprothesen oder Stents, Brachytherapiegeräte, Dialysatoren, chirurgische Laser, Nägel und Platten, externe Herzschrittmacher und Defibrillatoren, Lithotripter, Röntgengeräte, Kondome und Blutbeutel.
Die Übergangsfrist endet am 25. Mai 2023.
Klasse IIa
In der Klasse IIa befinden sich Medizinprodukte und Geräte mit mittlerem Risikopotenzial. Externe Hörgeräte, Kontaktlinsen, Blasenkatheter, Kanülen, OP-Handschuhe, diagnostischer Ultraschall, MRT, PET, TENS-Gerät und Zahnkronen gehören unteranderem in diese Klasse.
Die Übergangsfrist endet ebenfalls am 25. Mai 2023.
Klasse I
Die Klasse I ist die Klasse mit dem niedrigsten Risikopotenzial. In dieser Klasse befinden sich Gegenstände die zur Untersuchung oder dem täglichen Leben der Patienten helfen. Wie beispielsweise Brillen, Stethoskope, Mundspatel, Urinflaschen, aber auch viele Verbandmittel, Halskrausen, Rollstühle, Gehhilfen, Patientenbetten, Inkontinenzeinlagen und Dekubitusmatratzen.
Die Übergangsfrist endet am 25. Mai 2025.
Umsetzen der Verordnung mithilfe von COSYS
Wie am Anfang bereits erwähnt, müssen neben der Klassifizierung die Produkte auch gekennzeichnet werden. Die Softwarelösung von COSYS unterstützt Sie bei der Meldung an die EUDAMED und bei den notwenigen Kontrollen der Produkte. Neben der Software auf mobilen Geräten bietet COSYS auch ein Backend an. Auf dem Backend können alle erfassten Daten eingesehen und verwaltet werden. So kann auch die Pflicht zur Dokumentation erfüllt werden.
Informieren Sie sich noch heute unter: https://www.cosys.de/pharma-eu-verordnung
Auch interessant:
Medical Device Regulation
In-vitro-Diagnostika
UDI-Code
EUDAMED
MDE Geräte